| » Статистика |
Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
|
билет 3
|
[ Скачать с сервера (40.5 Kb)
]
| 07.02.2010, 17:44 |
Билет 3.
1. Неметаллы, их положение в ПСХЭ Д.И.Менделеева, строение атомов ( на примере углерода, азота, кислорода, фтора). Отличие физических свойств неметаллов от металлов. Взаимодействие неметаллов от металлов. Взаимодействие неметаллов с простыми веществами ( на примере реакций соединения серы с металлами, водородом и кислородом).
*****
План ответа:
а) Положение в ПС.
б) Строение атомов неметаллов.
в)Физические свойства.
г) Химические свойства.
Ответ следует начать с характеристики положения неметаллов в ПС: если провести воображаемую диагональ от бора В к астату At, то неметаллы располагаются в главных подгруппах выше диагонали (т.е. в верхнем правом углу). К неметаллам относятся также водород Н и инертные газы.
Рассмотрим строения атомов неметаллов на примере углерода С, азота N, кислорода О, фтора F. По мере увеличения порядковых номеров атомов элементов и накопления электронов на внешнем слое у неметаллов одного периода усиливается способность принимать электроны от других атомов на свой внешний слой, т.е. неметаллические свойства элементов в периода увеличиваются. (рис.1)
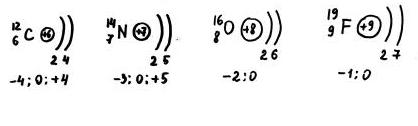
Рассматривая изменение свойств неметаллов при движении по группе, следует отметить, что они ослабевают. Это связано с увеличением расстояния от ядра до внешнего слоя, а следовательно, уменьшением способности ядра притягивать к себе электроны от других атомов. Для подтверждения этого вывода рассмотрим VI группу. В начале ее расположен кислород О – типичный неметалл, а заканчивается группа полонием Ро, обладающим свойствами металла.
Далее рассмотрим физические свойства неметаллов. Следует отметить, что простые вещества – неметаллы могут иметь как атомное (Si,B), так и молекулярное (Н2, N2, Br2) строение. Поэтому среди неметаллов есть газы (О2, Сl2), жидкости (Br2), твердые вещества (C, I2). Большинство неметаллов не электропроводны, имеют низкую теплопроводность, а твердые вещества непластичны.
Переходя к характеристике химических свойств, необходимо отметить, что более типичным для неметаллов является процесс принятия электронов. В этом отличие химических свойств неметаллов от химических свойств металлов. Это положение можно подтвердить взаимодействием неметаллов с простыми веществами. При этом следует записать уравнения соответствующих химических реакций и объяснить их сущность с точки зрения процессов окисления – восстановления. Следует отметить, что неметаллы могут проявлять свойства как окислителей, так и восстановителей. Приведем примеры.
1. Взаимодействие с металлами:
S + Fe = FeS
S0 +2e- = S-2 окислитель
Fe0 -2e- = Fe+2 восстановитель
2. Взаимодействие с неметаллами:
а) с водородом
S + Н2 = H2S
2H – 2e- =2H+1 восстановитель
S0 +2e- = S-2 окислитель
б) с кислородом
S0- 4e- = S+4 восстановитель
О2 + 2•2е- = 2О-2 окислитель
Можно добавить, что некоторые неметаллы могут реагировать и со сложными веществами (оксидами, кислотами, солями). Следующие уравнения можно привести в качестве примера (по желанию):
С + MgO = Mg + CO
Cl2 + 2FeCl2 = 2 FeCl3
C + 2H2SO4(конц) = СO2 + 2SO2 + 2 H2O
2. Задача. Определить какое количество вещества водорода получится, если в реакцию вступили натрий и вода массой 3,6 г
******
Можно использовать два способа решения этой задачи.
1 способ
1. Составим уравнение реакции:
2 Na + 2H2O = 2NaOH + H2↑
2. Находим количество вещества (n) воды:
n (Н2О) = m (H2O) / M(H2O) = 3,6 / 18 = 0,2 (моль)
3. Составляем и решаем пропорцию:
2 моль Н2О --- 1 моль Н2
0,2 моль Н2О --- х моль Н2
х = 0,2•1 / 2 = 0,1 (моль)
2 способ:
3,6 г х моль
2 Na + 2H2O = 2NaOH + H2
2•18= 36г/моль 1 моль
х = 3,6•1/36 = 0,1 (моль)
Ответ: образуется 0,1 моль водорода.
|
|
Категория: Экзаменационные билеты | Добавил: chimik
|
| Просмотров: 4204 | Загрузок: 363
| Рейтинг: 5.0/3 |
|
|
|